Au cours des dernières années, batteries lithium-ion Les batteries lithium-ion sont largement utilisées sur les marchés de la production et du stockage d'énergie. De ce fait, les ressources en lithium sont devenues de plus en plus rares. Les batteries sodium-ion fonctionnent selon un principe similaire et présentent des performances comparables à celles des batteries lithium-ion. Cependant, comparées à ces dernières, les batteries sodium-ion présentent plusieurs avantages indéniables :
- Abondantes réserves de matières premières
- Large distribution
- Faible coût
- Respect de l'environnement
- Compatibilité avec les systèmes existants équipement de production de batteries lithium-ion
Elles offrent également de bonnes performances énergétiques, une large plage de températures de fonctionnement, une sécurité élevée et aucune résistance à la décharge excessive. C'est pourquoi les batteries sodium-ion sont largement considérées comme une technologie alternative importante pour le stockage d'énergie à grande échelle.
Le rayon ionique de Na⁺ étant nettement supérieur à celui de Li⁺, les matériaux de cathode adaptés aux batteries lithium-ion ne conviennent pas nécessairement aux batteries sodium-ion. Le développement de matériaux de cathode présentant des canaux de transport ionique plus larges est donc devenu un facteur clé du progrès technologique des batteries sodium-ion.
Les principaux matériaux de cathode pour les batteries sodium-ion comprennent trois catégories :
- oxydes de métaux de transition
- composés polyanioniques
- Analogues du bleu de Prusse (ABP)
Parmi eux, les analogues du bleu de Prusse (ABP) ont suscité un vif intérêt. Ceci s'explique par leur structure ouverte unique et leurs larges canaux tridimensionnels. Ces caractéristiques offrent de nombreux sites de stockage du sodium et des voies d'insertion/extraction ioniques fluides. De ce fait, les ABP sont particulièrement adaptés à l'accueil et au stockage des ions Na⁺, plus volumineux.

Matériaux de cathode bleu de Prusse et analogues du bleu de Prusse
Le bleu de Prusse (BP) est un composé de coordination d'hexacyanoferrate de fer, représenté par Fe³⁺₄[Fe²⁺(CN)₆]₃⁻ ou Fe²⁺[Fe³⁺(CN)₆]₃⁻, abrégé en Fe-HCF. Sans modifier la structure globale du BP, le remplacement du fer par d'autres éléments métalliques donne naissance à une classe de nouveaux composés généralement appelés analogues du bleu de Prusse (ABP).
La formule structurale générale des PBA est :
NaxM[Fe(CN)₆]₁–y·□y·zH₂O
où M représente des éléments métalliques de transition tels que Fe, Co, Ni ou Mn ; □ désigne les lacunes Fe(CN)₆ ; 0 < x < 2 ; et 0 < y < 1.
La structure cristalline des PBA présente un réseau tridimensionnel ouvert unique. Elle se forme par coordination entre le métal de transition M et le fer avec les atomes d'azote et de carbone de CN⁻, respectivement. Les ions Na⁺ occupent les sites interstitiels, tandis que l'eau cristalline est présente à la surface et à l'intérieur des cristaux.
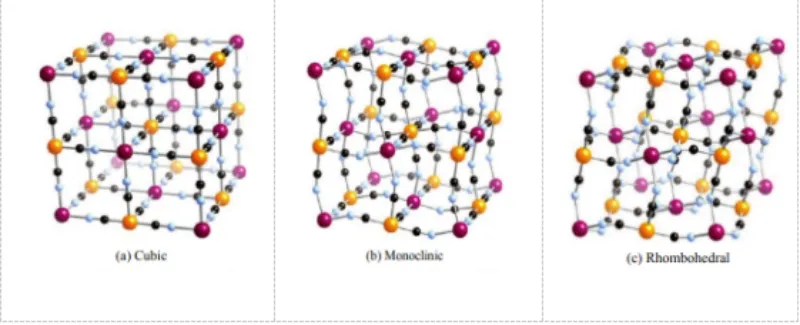
Les PBA présentent généralement une structure cubique à faces centrées. Cependant, les différences de procédés de préparation entraînent des variations de la teneur en Na⁺ et en eau de cristallisation. Ces variations peuvent déformer la structure cristalline et la conduire vers des systèmes monocliniques ou rhomboédriques. Lorsque le métal de transition M lié à l'atome d'azote CN⁻ change, les performances électrochimiques du matériau varient également.
Si M est électrochimiquement inactif, comme Ni, Zn ou Cu, un seul ion Na⁺ peut s'insérer et s'extraire de manière réversible lors des cycles. La capacité théorique est d'environ 85 mAh/g. Si M est électrochimiquement actif, comme Fe, Co ou Mn, deux ions Na⁺ peuvent participer à des réactions réversibles. La capacité théorique peut alors atteindre environ 170 mAh/g.
Les analogues du bleu de Prusse présentent de nombreux avantages en tant que matériaux de cathode pour les batteries sodium-ion, notamment :
- Une structure de canal tridimensionnelle de grande taille et de nombreux sites de stockage, facilitant la migration et le stockage du Na⁺.
- Une structure rigide avec un changement de volume minimal lors de l'insertion/extraction de Na⁺, conduisant à une bonne stabilité cyclique.
- Faibles barrières énergétiques de migration pour Na⁺, permettant un transport ionique rapide et améliorant la densité de puissance.
- Certains matériaux modifiés possèdent deux paires d'électrons redox, ce qui leur confère une capacité spécifique élevée.
- Procédé de synthèse simple et peu coûteux, adapté à une production à grande échelle.
- Écologique, non toxique et sans pollution.
Cependant, les PBA contiennent souvent une quantité considérable d'eau cristalline et des défauts structuraux de Fe(CN)₆ après synthèse. L'eau de réseau peut occuper les sites de stockage du sodium et les canaux de diffusion, réduisant ainsi la teneur en Na et ralentissant la migration ionique. Ceci affaiblit les performances électrochimiques. De plus, l'eau de coordination et les lacunes de Fe(CN)₆ dans la structure MHCF peuvent induire un effondrement structural lors des cycles, réduisant ainsi la stabilité. Par conséquent, les chercheurs continuent d'optimiser les voies de synthèse et d'appliquer des stratégies de modification afin d'obtenir des PBA à faible teneur en eau, présentant moins de défauts, une cristallinité élevée et des performances électrochimiques améliorées.
Méthodes de préparation des matériaux de cathode analogues au bleu de Prusse
Actuellement, les principales méthodes de synthèse des PBA utilisées dans les batteries sodium-ion se classent en deux catégories : les méthodes en phase liquide et les méthodes en phase solide. Les méthodes en phase liquide comprennent principalement la coprécipitation et les méthodes hydrothermales, tandis que les méthodes en phase solide reposent essentiellement sur le broyage mécanique à billes.
Parmi ces méthodes, la coprécipitation se distingue par sa simplicité de mise en œuvre, sa bonne maîtrise du procédé et sa capacité à permettre une production continue à grande échelle. Elle présente un potentiel d'application industrielle important et constitue actuellement la méthode privilégiée par les universités, les instituts de recherche et les entreprises industrielles pour l'étude des performances et la production en série de matériaux de cathode PBA.
3.1 Méthode de coprécipitation
La méthode de coprécipitation est la plus ancienne et la plus couramment utilisée pour la synthèse des PBA. Les premières préparations reposaient principalement sur une précipitation rapide. Des études ultérieures ont révélé que la cristallinité des PBA influence directement leurs performances électrochimiques. Afin d'améliorer la cristallinité, des méthodes de coprécipitation lente assistées par un agent chélateur ont été introduites.
Les agents chélateurs courants comprennent le citrate trisodique, l'oxalate de sodium, le pyrophosphate de sodium et l'acide éthylènediaminetétraacétique (EDTA).
Outre la cristallinité, la teneur en eau cristalline, les défauts structuraux et la teneur en sodium des structures MHCF influent également de manière significative sur leurs performances électrochimiques. Afin de réduire la teneur en eau cristalline, les chercheurs optimisent les méthodes de séchage, introduisent des additifs, modifient la formulation des solvants et ajustent la durée et la température de la réaction.
Bien que la coprécipitation lente prenne du temps, elle permet un ajustement facile du processus et permet la synthèse de PBA à haute cristallinité, faible teneur en eau, faible défaut et haute teneur en sodium avec d'excellentes performances électrochimiques.
3.2 Méthode hydrothermale
Outre la coprécipitation, la méthode hydrothermale a également été appliquée avec succès à la synthèse de PBA (notamment de FeHCF). Liu et al. ont utilisé différentes concentrations de HCl dans un procédé hydrothermal pour synthétiser du FeHCF présentant des morphologies variées.
L'ajout de 1 mL d'HCl a permis d'obtenir des particules cubiques de FeHCF. Avec 2 mL d'HCl, la surface des particules est devenue légèrement rugueuse. À 3 mL, leur morphologie s'est transformée en particules sphériques. Les particules cubiques de FeHCF ont présenté les meilleures performances électrochimiques, avec une capacité de 107 mAh/g à 0,2 A/g et une rétention de capacité de 741 TP3T après 500 cycles. Même à une densité de courant élevée de 5 A/g, elles ont conservé une capacité de 82 mAh/g.
3.3 Broyeur à billes Méthode

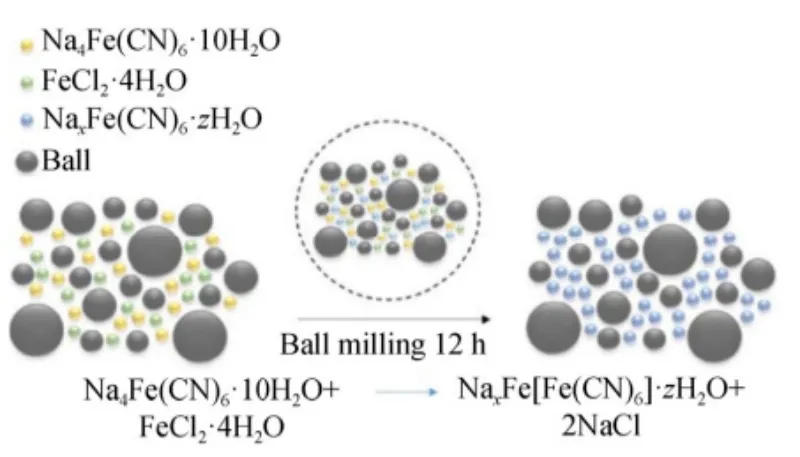
Le broyage à billes utilise les vibrations et les chocs mécaniques pour réduire les grosses particules en poudres nanométriques. Il convient à la synthèse de matériaux à faible teneur en eau interstitielle. Le procédé est simple et permet de réduire l'eau de cristallisation et la taille des particules.
Cependant, les particules primaires obtenues par cette méthode ont tendance à s'agglomérer, les réactions solide-solide peuvent être incomplètes et des impuretés peuvent être introduites. De plus, les matériaux synthétisés par broyage à billes sont actuellement relativement peu nombreux et se concentrent principalement sur le FeHCF.
Modification des matériaux de cathode analogues au bleu de Prusse
Outre l'optimisation des procédés de synthèse, les PBA peuvent être modifiés par la formation de composites avec d'autres matériaux ou par dopage ionique.
4.1 Modification composite
Les PB et les PBA peuvent être combinés avec d'autres matériaux (tels que des matériaux carbonés, des polymères organiques et du graphène) pour obtenir des composites de cathode avec une conductivité améliorée, un transport d'ions plus rapide, des performances de vitesse améliorées et une durée de vie cyclique plus longue.
Composite avec des matériaux en carbone
Les matériaux carbonés sont largement utilisés non seulement comme matériaux d'électrode actifs, mais aussi comme matrices conductrices en raison de leur conductivité électronique élevée. Ils améliorent la conductivité, limitent l'agrégation des particules, renforcent la stabilité structurale lors des cycles de charge/décharge et servent de matrice tampon pour atténuer la dilatation de l'électrode lors de l'insertion/extraction des ions Na⁺. Ainsi, la fabrication d'électrodes composites à base de matériaux carbonés constitue une stratégie efficace pour améliorer les performances électrochimiques.
Composite avec des polymères conducteurs organiques
Les polymères conducteurs organiques (tels que la polyaniline, le polypyrrole et le poly(3,4-éthylènedioxythiophène)) présentent des avantages comme une capacité de stockage d'énergie élevée, un faible coût, des propriétés physico-chimiques modulables et une bonne stabilité environnementale. L'incorporation de ces polymères dans les PBA constitue une méthode efficace pour améliorer leurs performances électrochimiques.
Composite avec du graphène
La plupart des matériaux PB et PBA présentent une faible conductivité et une instabilité structurelle. Le graphène, grâce à ses excellentes propriétés électrochimiques, sa grande surface spécifique, ses nombreux sites de bord et ses défauts, facilite le transport rapide des ions sodium et améliore considérablement la conductivité lorsqu'il est combiné aux PB/PBA.
4.2 Modification du dopage
Le dopage est une autre stratégie de modification courante. Un dopage approprié peut réduire la bande interdite et les barrières d'énergie de migration, améliorant ainsi la mobilité des électrons et des ions Na⁺.
Le dopage avec des ions métalliques de rayon plus important permet d'augmenter les paramètres de maille, le nombre de sites de stockage du sodium et la largeur des canaux de diffusion des ions Na⁺. L'introduction d'ions métalliques électrochimiquement actifs peut accroître la capacité, tandis que l'incorporation d'ions métalliques électrochimiquement inactifs peut servir de piliers structuraux pour améliorer la stabilité cyclique.
Pour les PBA, le dopage est généralement effectué au niveau du site du métal de transition coordonné à l'azote. Le NiHCF présentant une excellente stabilité cyclique, le dopage au Ni est souvent utilisé pour modifier les matériaux de cathode FeHCF, MnHCF et CoHCF.

Conclusion
Les matériaux de cathode analogues au bleu de Prusse présentent d'excellentes performances de stockage du sodium grâce à leur structure à réseau ouvert unique, à leurs nombreux sites de stockage du sodium et à leurs larges canaux de migration des ions sodium. Cependant, lors de la synthèse, de l'eau cristalline et des lacunes de Fe(CN)₆ se forment facilement, ce qui affecte considérablement leurs performances électrochimiques.
Bien que l'optimisation des procédés de synthèse, la formation de composites avec d'autres matériaux et l'application du dopage ionique puissent améliorer les performances de stockage du sodium, des recherches supplémentaires sont encore nécessaires pour parvenir à une production industrielle à grande échelle.

« Merci de votre lecture. J’espère que cet article vous sera utile. N’hésitez pas à laisser un commentaire ci-dessous. Pour toute question, vous pouvez également contacter le service client en ligne de Zelda. »
— Publié par Emily Chen
